

Vihuma
simoctocog alfa
Säilytä tämä pakkausseloste. Voit tarvita sitä myöhemmin.
Jos sinulla on kysyttävää, käänny lääkärin puoleen.
Tämä lääke on määrätty vain sinulle eikä sitä pidä antaa muiden käyttöön. Se voi aiheuttaa haittaa muille, vaikka heillä olisikin samanlaiset oireet kuin sinulla.
Jos havaitset haittavaikutuksia, kerro niistä lääkärille. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Ks. kohta 4.
Mitä Vihuma on ja mihin sitä käytetään
Mitä sinun on tiedettävä, ennen kuin käytät Vihuma-valmistetta
Miten Vihuma-valmistetta käytetään
Mahdolliset haittavaikutukset
Vihuma-valmisteen säilyttäminen
Pakkauksen sisältö ja muuta tietoa
Vihuma-valmisteen vaikuttava aine on rekombinantti ihmisen veren hyytymistekijä VIII (kutsutaan myös simoktokogi alfaksi). Hyytymistekijä VIII on välttämätön veren hyytymiselle ja verenvuodon tyrehtymiselle. A-hemofiliaa (synnynnäinen hyytymistekijä VIII:n puutos) sairastavilla potilailla ei ole veressään lainkaan hyytymistekijä VIII:aa tai se ei toimi riittävän tehokkaasti.
Vihuma-valmiste korvaa puuttuvan hyytymistekijä VIII:n, jotta veren hyytyminen voi tapahtua normaalisti, ja sitä voidaan käyttää kaikissa ikäryhmissä verenvuotojen hoitoon ja ennaltaehkäisyyn A- hemofiliaa sairastaville potilaille.
jos olet allerginen vaikuttavalle aineelle simoktokogi alfalle tai tämän lääkkeen jollekin muulle aineelle (lueteltu kohdassa 6).
Jos olet epävarma, kysy neuvoa lääkäriltä.
Keskustele lääkärin kanssa ennen kuin käytät Vihuma-valmistetta.
On epätodennäköistä mutta kuitenkin mahdollista, että Vihuma aiheuttaa sinulle anafylaktisen reaktion (äkillinen vakava allerginen reaktio). Siksi sinun on tunnettava allergisten reaktioiden ensioireet, jotka luetellaan kohdassa 4, Allergiset reaktiot.
Jos sinulle ilmaantuu jokin näistä oireista, lopeta lääkkeen ottaminen heti ja ota yhteys lääkäriin.
Inhibiittorien (vasta-aineiden) muodostuminen on tunnettu komplikaatio, joka voi kehittyä minkä tahansa tekijä VIII -lääkkeen käytön aikana. Etenkin suurina pitoisuuksina esiintyessään nämä inhibiittorit estävät hoitoa vaikuttamasta oikein, ja sinua tai lastasi seurataan huolellisesti inhibiittorien kehittymisen varalta. Kerro lääkärille heti, jos verenvuotosi tai lapsesi verenvuoto ei ole hallittavissa Vihuma-valmisteella.
Sydän- ja verisuonitapahtumat
Potilailla, joilla on sydän- ja verisuonitautien riskitekijöitä, korvaushoito hyytymistekijä VIII:lla voi lisätä sydän- ja verisuonitautien riskiä.
Katetreihin liittyvät komplikaatiot
Jos hoitosi edellyttää keskuslaskimokatetrin käyttöä, on otettava huomioon tähän liittyvien komplikaatioiden mahdollisuus. Niitä ovat mm. paikalliset infektiot, bakteerien esiintyminen veressä
ja katetrikohdan tromboosi.
Vihuma-valmisteen eränumeroiden kirjaaminen on tärkeää.
Aina kun saat uuden Vihuma-pakkauksen, merkitse päivämäärä ja eränumero (joka on merkitty pakkaukseen sanan {Lot} jälkeen) muistiin ja säilytä tiedot turvallisessa paikassa.
Kerro lääkärille, jos parhaillaan käytät tai olet äskettäin käyttänyt tai saatat käyttää muita lääkkeitä.
Jos olet raskaana tai imetät, epäilet olevasi raskaana tai jos suunnittelet lapsen hankkimista, kysy lääkäriltä neuvoa ennen tämän lääkkeen käyttöä.
Vihuma-valmisteella ei ole vaikutusta ajokykyysi ja kykyysi käyttää koneita.
Tämä lääke sisältää 18,4 mg natriumia (ruokasuolan toinen ainesosa) per injektiopullo. Tämä vastaa 0,92 %:a suositellusta natriumin enimmäisvuorokausiannoksesta aikuiselle.
Vihuma-hoidon aloittaa lääkäri, jolla on kokemusta A-hemofiliaa sairastavien potilaiden hoidosta. Käytä tätä lääkevalmistetta aina juuri kuten lääkäri tai sairaanhoitaja on neuvonut. Tarkista ohjeet lääkäriltä tai sairaanhoitajalta, jos olet epävarma.
Yleensä Vihuma-valmisteen ruiskuttaa laskimoon lääkäri tai sairaanhoitaja. Sinä itse tai joku muu voi myös antaa Vihuma-injektion mutta vasta asianmukaisen perehdytyksen jälkeen.
Lääkäri laskee Vihuma-annoksesi (kansainvälisinä yksikköinä = IU) kliinisen tilasi ja painosi mukaan. Annokseen vaikuttaa myös se, käytetäänkö lääkettä verenvuodon ennaltaehkäisyyn vai hoitoon. Se kuinka usein tarvitset injektion riippuu siitä, miten hyvin Vihuma tehoaa sinulle. Yleensä A- hemofilian hoito on koko eliniän mittainen.
Verenvuodon ennaltaehkäisy
Tavallinen Vihuma-annos on 20-40 IU painokiloa kohti joka toinen tai kolmas päivä. Joissakin tapauksissa, erityisesti nuorille potilaille, voivat lyhyemmät antovälit tai suuremmat annokset olla tarpeen.
Verenvuodon hoito
Vihuma-annos lasketaan painon ja tarvittavan hyytymistekijä VIII -pitoisuuden mukaan. Tarvittava hyytymistekijä VIII -pitoisuus riippuu verenvuodon vakavuudesta ja sijainnista.
Jos sinusta tuntuu, että Vihuma ei tehoa tarpeeksi hyvin, kerro siitä lääkärille. Lääkäri tekee tarvittavat laboratoriokokeet varmistaakseen, että veresi hyytymistekijä VIII -pitoisuus on riittävä. Tämä on erityisen tärkeää, jos olet menossa suureen leikkaukseen.
Potilaat, joille muodostuu hyytymistekijä VIII:n inhibiittoreita
Jos hyytymistekijä VIII -pitoisuus ei nouse Vihuma-valmisteella riittävästi tai jos verenvuotoa ei saada riittävän hyvin hallintaan, tämä saattaa johtua hyytymistekijä VIII:n inhibiittorien (vasta-aineiden)
muodostumisesta. Lääkärisi tutkii, onko asia näin. Saatat tarvita suuremman annoksen Vihuma- valmistetta tai toisen valmisteen verenvuotojen hoitoon. Älä yritä hoitaa verenvuotoa Vihuma-
valmisteen kokonaisannosta lisäämällä keskustelematta ensin lääkärin kanssa.
Vihuma-valmisteen käyttötapa lapsille ja nuorille ei poikkea käytöstä aikuisille. Koska hyytymistekijä VIII -valmisteita saatetaan joutua antamaan lapsille ja nuorille useammin, voi olla tarpeen asentaa keskuslaskimokatetri (CVAD). CVAD on elimistön ulkopuolinen laite, jonka avulla lääkkeitä voidaan antaa verenkiertoon ilman ihon läpi tapahtuvaa injektiota.
Yliannostusoireita ei ole raportoitu. Jos olet käyttänyt enemmän Vihuma-valmistetta kuin sinun pitäisi, kerro siitä lääkärille.
Älä ota kaksinkertaista annosta korvataksesi unohtamasi kerta-annoksen. Ota seuraava annos heti ja jatka hoitoa lääkärin neuvojen mukaan.
Älä lopeta Vihuma-valmisteen käyttöä keskustelematta ensin lääkärin kanssa.
Jos sinulla on kysymyksiä tämän lääkkeen käytöstä, käänny lääkärin tai sairaanhoitajan puoleen.
Kuten kaikki lääkkeet, tämäkin lääke voi aiheuttaa haittavaikutuksia. Kaikki eivät kuitenkaan niitä saa.
Allergisia reaktioita voivat olla ihottuma, nokkosihottuma (kutiseva ihottuma), mukaan lukien yleistynyt nokkosihottuma, huulten ja kielen turpoaminen, hengenahtistus, hengityksen
vinkuminen, puristava tunne rinnassa, oksentelu, levottomuus, matala verenpaine ja
heitehuimaus. Nämä voivat olla anafylaktisen sokin ensioireita. Jos voimakkaita, äkillisiä allergisia (anafylaktisia) reaktioita ilmenee, injektio on keskeytettävä heti, ja lääkäriin on otettava yhteyttä välittömästi. Vakavat oireet edellyttävät kiireellistä hoitoa.
Lapsille ja nuorille, jotka eivät ole aiemmin saaneet tekijä VIII -lääkkeitä, kehittyy hyvin yleisesti (yli yhdellä potilaalla 10:stä) inhibiittoreita eli vasta-aineita (ks. kohta 2).
Riski on kuitenkin melko harvinainen (alle yhdellä potilaalla 100:sta), jos potilas on saanut
aiemmin tekijä VIII -hoitoa (yli 150 hoitopäivää). Tällöin lääkityksesi tai lapsesi lääkitys voi lakata vaikuttamasta oikein, ja sinulla tai lapsellasi voi esiintyä jatkuvaa verenvuotoa. Jos näin käy, lääkäriin on otettava heti yhteyttä.
Yliherkkyys, kuume.
Kihelmöinti tai puutuminen (parestesia), päänsärky, kiertohuimaus, suun kuivuminen, heitehuimaus, injektiokohdan tulehdus, kipu injektiokohdassa, lievä huonovointisuus, verenvuodosta johtuva anemia, positiivinen ei-neutraloiva vasta-aine (aiemmin hoidetut potilaat).

Jos havaitset haittavaikutuksia, kerro niistä lääkärille. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Voit ilmoittaa haittavaikutuksista
myös suoraan liitteessä V luetellun kansallisen ilmoitusjärjestelmän kautta. Ilmoittamalla haittavaikutuksista voit auttaa saamaan enemmän tietoa tämän lääkevalmisteen turvallisuudesta.
Ei lasten ulottuville eikä näkyville.
Älä käytä tätä lääkettä kotelon ja injektiopullon etiketissä mainitun viimeisen käyttöpäivämäärän (EXP) jälkeen. Viimeinen käyttöpäivämäärä tarkoittaa kuukauden viimeistä päivää.
Säilytä jääkaapissa (2 °C – 8 °C). Ei saa jäätyä. Säilytä injektiopullo alkuperäispakkauksessa. Herkkä valolle.
Ennen Vihuma-kuiva-aineen liuottamista se voidaan pitää huoneenlämmössä (enintään 25 °C) yhtäjaksoisesti enintään 1 kuukauden ajan. Merkitse Vihuma-koteloon päivämäärä, jolloin valmisteen huoneenlämpösäilytys alkaa. Älä säilytä Vihuma-valmistetta enää jääkaapissa sen jälkeen, kun sitä on säilytetty huoneenlämmössä.
Käytä liuos välittömästi käyttökuntoon saattamisen jälkeen.
Älä käytä tätä lääkettä, jos huomaat näkyviä muutoksia pakkauksen suojauksessa, erityisesti ruiskun ja/tai injektiopullon suojauksessa.
Lääkkeitä ei pidä heittää viemäriin eikä hävittää talousjätteiden mukana. Kysy käyttämättömien lääkkeiden hävittämisestä apteekista. Näin menetellen suojelet luontoa.
Injektiokuiva-aine:
Vaikuttava aine on rekombinantti ihmisen veren hyytymistekijä VIII (simoktokogi alfa).
Yksi injektiopullo injektiokuiva-ainetta sisältää 250, 500, 1000, 2000, 2500, 3000 tai 4000 IU simoktokogi alfaa.
Yksi käyttökuntoon saatettu liuos sisältää noin 100, 200, 400, 800, 1000, 1200 tai 1600 IU/ml simoktokogi alfaa.
Muut aineet ovat sakkaroosi, natriumkloridi, kalsiumklorididihydraatti, arginiinihydrokloridi,
natriumsitraattidihydraatti ja poloksameeri 188. Ks. kohta 2, "Vihuma sisältää natriumia".
Liuotin:
Injektionesteisiin käytettävä vesi
Vihuma on injektiokuiva-aine ja liuotin liuosta varten. Kuiva-aine on valkoinen tai luonnonvalkoinen jauhe lasisessa injektiopullossa. Liuotin on injektionesteisiin käytettävää vettä esitäytetyssä
lasiruiskussa. Käyttökuntoon saattamisen jälkeen valmis liuos on kirkas ja väritön eikä siinä ole
ylimääräisiä hiukkasia.
Yksi Vihuma -pakkaus sisältää:
1 injektiokuiva-ainepullo, jossa on 250, 500, 1000, 2000, 2500, 3000 tai 4000 IU simoktokogi alfaa.
1 esitäytetty ruisku, jossa on 2,5 ml injektionesteisiin käytettävää vettä
1 injektiopullon adapteri
1 perhosneula
2 alkoholilla kostutettua pyyhettä
Octapharma AB, Lars Forssells gata 23, 112 75 Stockholm, Ruotsi
Lisätietoja tästä lääkevalmisteesta antaa myyntiluvan haltijan paikallinen edustaja:
Biotest AG (Germany) Tel: +49 6103 801-0
Biotest AG (Germany)
Teл.: +49 6103 801-0
Biotest AG (Germany) Tel: +49 6103 801-0
Biotest AG (Germany) Tlf: +49 6103 801-0
Biotest AG (Germany) Tel: +49 6103 801-0
Biotest AG (Germany) Tel: +49 6103 801-0
Biotest AG (Germany) Tel: +49 6103 801-0
Biotest AG (Germany) Tel: +49 6103 801-0
Biotest AG (Germany) Tlf: +49 6103 801-0
Biotest AG (Germany)
Τηλ: +49 6103 801-0
Biotest Austria GmbH Tel: +43 1 545 15 61-0
Biotest AG (Germany) Tel: +49 6103 801-0
Biotest AG (Germany) Tel: +49 6103 801-0
Biotest AG (Germany) Tél: +49 6103 801-0
Biotest AG (Germany) Tel: +49 6103 801-0
Biotest AG (Germany) Tél: +49 6103 801-0
Biotest AG (Germany) Tel: +49 6103 801-0
Biotest AG (Germany) Tel: +49 6103 801-0
Biotest AG (Germany) Tel: +49 6103 801-0
Biotest AG (Germany) Sími: +49 6103 801-0
Biotest AG (Germany) Tel: +49 6103 801-0
Biotest AG (Germany) Tel: +49 6103 801-0
Biotest AG (Germany) Puh/Tel: +49 6103 801-0
Biotest AG (Germany)
Τηλ: +49 6103 801-0
Biotest AG (Germany) Tel: +49 6103 801-0
Biotest AG (Germany) Tel: +49 6103 801-0
Biotest AG (Germany) Tel: +49 6103 801-0
---------------------------------------------------------------------------------------------------------------------------
Seuraavat tiedot on tarkoitettu vain hoitoalan ammattilaisille: Hoito tarvittaessa
Annettavalla määrällä ja antotiheydellä pyritään aina jokaisessa tapauksessa kliinisen tehon
varmistamiseen. Seuraavissa verenvuototapahtumissa hyytymistekijä VIII -aktiivisuus ei saa laskea alle plasman annetun aktiivisuustason (prosenttia normaalitasosta tai IU/dl) vastaavana ajanjaksona.
Seuraavaa taulukkoa voidaan käyttää annostelun ohjeena verenvuodoissa ja leikkauksissa.



Verenvuoto
Varhaisvaiheen nivelensisäinen, lihaksen tai suun verenvuoto

Suurehko nivelensisäinen vuoto, lihasverenvuoto tai verenpurkauma
20–40 Toistetaan 12–24 tunnin välein.
Vähintään vuorokauden ajan, kunnes tilanne on ohi (kipu hävinnyt, vuoto loppunut).
30–60 Infuusio toistetaan 12–24 tunnin välein
3–4 vuorokauden ajan tai kauemmin, kunnes kipu ja akuutti haitta ovat
helpottaneet.

Hengenvaaralliset verenvuodot 60–100 Infuusio toistetaan 8–24 tunnin välein,

kunnes vaara on ohi.

Leikkaus Pieni leikkaus,
mukaan lukien hampaanpoisto

30–60 24 tunnin välein vähintään vuorokauden ajan, kunnes potilas on toipunut.
Suuri leikkaus 80–100
(ennen leikkausta ja sen jälkeen)
Infuusio toistetaan 8–24 tunnin välein, kunnes haava on riittävästi parantunut. Tämän jälkeen hoitoa jatketaan vielä vähintään 7 vuorokautta, jotta tekijä VIII -aktiivisuus pysyy tasolla 30– 60% (IU/dl).

Anna liuotinruiskun (injektionesteisiin käytettävä vesi) ja suljetussa injektiopullossa olevan injektiokuiva-aineen lämmetä huoneenlämpöisiksi. Voit tehdä sen pitämällä niitä käsissäsi niin kauan, että ne tuntuvat yhtä lämpimiltä kuin kätesi. Älä käytä mitään muuta keinoa injektiopullon ja esitäytetyn ruiskun lämmittämiseksi. Niiden tulee pysyä huoneenlämpöisinä käyttökuntoon saattamisen aikana.
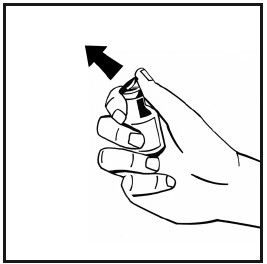
Poista muovinen repäisykorkki injektiokuiva-ainepullosta, niin että kumitulpan keskiosa tulee näkyviin. Älä poista harmaata tulppaa äläkä metallirengasta injektiopullon yläosan ympäriltä.
Pyyhi injektiopullon yläosa alkoholilla kostutetulla pyyhkeellä. Anna alkoholin kuivua.
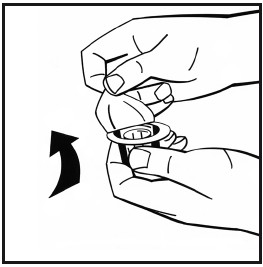
Vedä injektiopullon adapterin pakkauksen paperinen suojapäällinen pois. Jätä adapteri pakkaukseen.
Pane injektiokuiva-ainepullo tasaiselle alustalle ja pidä sitä paikoillaan. Ota adapteripakkaus ja aseta injektiopullon adapteri injektiokuiva-ainepullon kumisen tulpan keskikohdan päälle. Paina adapteripakkausta lujasti alaspäin, kunnes adapterin kärki puhkaisee kumitulpan. Adapteri napsahtaa kiinni injektiopulloon.
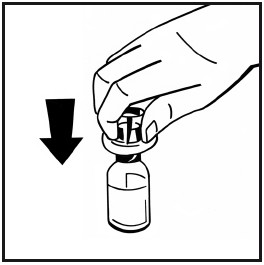
Vedä esitäytetyn ruiskun pakkauksen paperinen suojapäällinen pois. Pidä kiinni ruiskun
männän päästä äläkä koske männän varteen. Kiinnitä ruiskun männän kierteinen pää liuotinruiskuun kiertämällä mäntää myötäpäivään, kunnes tunnet pienen vastuksen.
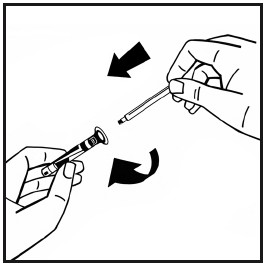
Katkaise liuotinruiskun toisen pään suojattu muovipää korkin perforoinnin kohdalta. Älä koske korkin sisäpuoleen äläkä ruiskun päähän.

Poista adapterin pakkaus injektiopullon kärjestä ja heitä se pois.
Kiinnitä liuotinruisku lujasti injektiopullon adapteriin kiertämällä myötäpäivään, kunnes tunnet vastuksen.

Ruiskuta kaikki liuotin hitaasti injektiokuiva-ainepulloon painamalla ruiskun mäntä alas.

Älä poista ruiskua. Liikuttele tai pyörittele injektiopulloa varovasti muutaman kerran niin, että injektiokuiva-aine liukenee. Ei saa ravistaa. Odota, kunnes injektiokuiva-aine on kokonaan liuennut.
Ennen lääkkeen antamista tarkista, ettei liuoksessa ole näkyviä hiukkasia. Liuoksen on oltava kirkas ja väritön eikä siinä saa olla näkyviä hiukkasia. Älä käytä liuosta, joka on samea tai
jossa on saostumia.
Käännä ruiskuun kiinnitetty injektiopullo ylösalaisin ja vedä valmis liuos hitaasti ruiskuun.
Varmista, että kaikki injektiopullon sisältö siirtyy ruiskuun.
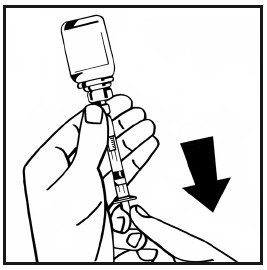
Irrota täytetty ruisku injektiopullon adapterista kiertämällä injektiopulloa vastapäivään ja heitä tyhjä injektiopullo pois.
Liuos on nyt valmis, ja se pitää käyttää välittömästi. Älä säilytä kylmässä.
Puhdista valittu injektiokohta alkoholilla kostutetulla pyyhkeellä, joka on pakkauksessa.
Liitä infuusiolaitteisto ruiskuun.
Työnnä infuusiolaitteiston neula valittuun laskimoon, kuten sinua on neuvottu. Jos olet käyttänyt kiristyssidettä suonen löytämiseksi, poista kiristysside ennen kuin alat ruiskuttaa liuosta.
Ruiskuun ei saa päästä verta, sillä se voi muodostaa hyytymän ja tukkia ruiskun, jolloin oikean annoksen pistäminen ei onnistu.
Ruiskuta liuos hitaasti laskimoon, enintään 4 ml minuutissa.
Jos käytät useamman kuin yhden injektiokuiva-ainepullollisen hoitokerran aikana, voit käyttää samaa infuusiolaitteiston injektioneulaa uudelleen. Injektiopullon adapteri ja ruisku ovat kertakäyttöisiä.