

Varilrix
varicella, live attenuated
Kylmäkuivattuja, heikennettyjä, eläviä varicella-zosterviruksia sisältävä vesirokkorokote Vesirokkorokote (elävä)
Säilytä tämä pakkausseloste. Voit tarvita sitä myöhemmin.
Jos sinulla on kysyttävää, käänny lääkärin, apteekkihenkilökunnan tai sairaanhoitajan puoleen.
Tämä rokote on määrätty vain sinulle tai lapsellesi eikä sitä pidä antaa muiden käyttöön.
Jos havaitset itselläsi tai lapsellasi haittavaikutuksia, kerro niistä lääkärille, apteekkihenkilökunnalle tai sairaanhoitajalle. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Ks. kohta 4.
Mitä Varilrix on ja mihin sitä käytetään
Mitä sinun on tiedettävä, ennen kuin saat / lapsesi saa Varilrix-valmistetta
Miten Varilrix-valmistetta annetaan
Mahdolliset haittavaikutukset
Varilrix-valmisteen säilyttäminen
Pakkauksen sisältö ja muuta tietoa
Varilrix on vähintään 12 kuukauden ikäisille tarkoitettu rokote vesirokkoa vastaan. Rokotetta voidaan antaa erityistapauksissa pikkulapsille 9 kuukauden iästä alkaen.
Rokotus, joka annetaan 3 päivän kuluessa vesirokkoaltistuksesta, saattaa ehkäistä vesirokkoa tai lieventää sen vaikeusastetta.
Varilrix-rokotuksen jälkeen immuunijärjestelmä (elimistön luontainen puolustusjärjestelmä) alkaa kehittää vasta-aineita, jotka suojaavat rokotettua henkilöä vesirokkotartunnalta.
Varilrix sisältää heikennettyjä viruksia. On erittäin epätodennäköistä, että ne aiheuttaisivat terveillä henkilöillä vesirokon.
Muiden rokotteiden tavoin Varilrix ei välttämättä tuota kaikille rokotetuille täydellistä suojaa.
jos sinä sairastat / lapsesi sairastaa immuunijärjestelmää heikentävää tautia (esim. veritauti, syöpä, HIV [immuunikatovirus], AIDS [immuunikatotauti]) tai jos sinä käytät / lapsesi käyttää immuunijärjestelmää heikentävää lääkettä (esim. suuriannoksinen kortikosteroidihoito). Immuunipuolustuksen taso ratkaisee, annetaanko sinulle/lapsellesi rokote. Ks. kohta 2 ”Varoitukset ja varotoimet”.
jos sinä olet tai lapsesi on allerginen tämän rokotteen jollekin aineelle (lueteltu kohdassa 6). Allergisen reaktion merkkejä voivat olla kutiava ihottuma, hengenahdistus ja kasvojen tai
kielen turvotus.
jos sinä olet tai lapsesi on allerginen neomysiinille (antibiootti). Tiedossa oleva kontakti- ihottuma (ihottuma suoran allergeenikontaktin kuten neomysiinikontaktin jälkeen) ei yleensä ole este rokottamiselle, mutta keskustele asiasta ensin lääkärin kanssa.
jos sinulle tai lapsellesi on kehittynyt allerginen reaktio jonkin aikaisemman vesirokkorokotteen yhteydessä.
jos olet raskaana. Raskautta on lisäksi vältettävä yhden kuukauden ajan rokotuksen jälkeen.
Keskustele lääkärin, apteekkihenkilökunnan tai sairaanhoitajan kanssa ennen kuin sinulle/lapsellesi annetaan Varilrix-valmistetta:
jos sinulla tai lapsellasi on vaikea infektio, johon liittyy korkea kuume. Rokotusta voi olla tarpeen siirtää infektion paranemiseen saakka. Lievä infektio kuten nuhakuume ei yleensä edellytä rokotuksen siirtämistä, mutta keskustele asiasta ensin lääkärin kanssa.
jos sinulla tai lapsellasi on heikentynyt immuunijärjestelmä jonkin sairauden (esim. HIV- infektion vuoksi) ja/tai jonkin hoidon vuoksi. Sinua tai lastasi seurataan huolellisesti, sillä rokotteen aikaansaama vaste ja suoja tautia vastaan saattaa jäädä puutteelliseksi (ks. kohta 2 ”Varilrixia ei saa antaa”).
jos sinulla on verenvuotohäiriö tai saat herkästi mustelmia.
Pyörtyminen on mahdollista etenkin nuorilla minkä tahansa neulanpiston jälkeen ja jopa ennen neulanpistoa. Kerro siis lääkärille tai sairaanhoitajalle, jos olet pyörtynyt tai lapsesi on joskus pyörtynyt pistoksen yhteydessä.
Muiden rokotteiden tavoin Varilrix ei välttämättä anna sinulle tai lapsellesi täydellistä suojaa vesirokkoa vastaan. Rokotuksen saaneilla vesirokko on kuitenkin yleensä hyvin lievä verrattuna rokottamattomiin.
Heikennetty virus voi harvinaisissa tapauksissa tarttua rokotetusta henkilöstä muihin ihmisiin. Tällöin rokotetulla henkilöllä on yleensä esiintynyt näppylöitä tai rakkuloita. Tällä tavalla tartunnan saaneille terveille henkilöille kehittyy yleensä vain lievä ihottuma, joka ei aiheuta haittaa.
Kun sinulle tai lapsellesi on annettu rokote, lähikontaktia seuraaviin ryhmiin on vältettävä mahdollisuuksien mukaan 6 viikon ajan rokottamisen jälkeen:
Henkilöt, joiden immuunipuolustus on heikentynyt
Raskaana olevat naiset, jotka eivät ole sairastaneet vesirokkoa tai joita ei ole rokotettu vesirokkoa vastaan
Vastasyntyneet, joiden äiti ei ole sairastanut vesirokkoa tai joiden äitiä ei ole rokotettu vesirokkoa vastaan.
Kerro lääkärille tai apteekkihenkilökunnalle, jos parhaillaan otat, olet äskettäin ottanut tai saatat ottaa muita rokotteita ja/tai lääkkeitä. Tämä pätee myös lapseesi.
Kerro lääkärille, jos sinulle tai lapsellesi aiotaan tehdä tuberkuloosia kartoittava ihotesti. Jos tämä testi tehdään 6 viikon kuluessa Varilrixin annosta, testitulos ei välttämättä ole luotettava.
Rokotusta on siirrettävä vähintään 3 kuukautta, jos sinulle tai lapsellesi on annettu verensiirto tai ihmisen omia vasta-aineita (immunoglobuliineja).
Salisylaattien käyttöä (käytetään lievittämään kipua ja kuumetta; esim. Aspirin®) on vältettävä 6 viikon ajan Varilrix-rokotuksen jälkeen, sillä seurauksena saattaa olla vakava tauti, Reyesin oireyhtymä, joka voi vaikuttaa kaikkiin elimiin.
Varilrix voidaan antaa samanaikaisesti muiden rokotteiden kanssa. Kukin rokote annetaan kuitenkin eri kohtaan.
Varilrixia ei saa antaa raskaana oleville naisille.
Jos olet raskaana tai imetät, epäilet olevasi raskaana tai jos suunnittelet lapsen hankkimista, kysy lääkäriltä tai apteekista neuvoa ennen rokotusta. On myös tärkeää, että et tule raskaaksi kuukauden sisällä rokotuksesta. Tänä aikana sinun on käytettävä tehokasta ehkäisyä raskauden välttämiseksi.
Kerro lääkärille, jos imetät tai aiot imettää. Lääkäri päättää, voitko saada Varilrixia.
Varilrix-valmisteella ei ole tai sillä on vain vähäinen vaikutus ajokykyyn ja koneidenkäyttökykyyn. Kuitenkin jotkin kohdassa 4. ”Mahdolliset haittavaikutukset” mainituista vaikutuksista voivat vaikuttaa tilapäisesti ajokykyyn tai koneidenkäyttökykyyn.
Tämä lääkevalmiste sisältää 6 mg sorbitolia per annos.
Tämä lääkevalmiste sisältää 331 mikrogrammaa fenyylialaniinia per annos. Fenyylialaniini voi olla haitallista, jos sinulla on fenyyliketonuria (PKU), harvinainen perinnöllinen sairaus, jossa kertyy fenyylialaniinia, koska elimistö ei kykene poistamaan sitä kunnolla.
Varilrix annetaan pistoksena ihon alle tai lihakseen joko olkavarteen tai ulkoreiteen.
Vähintään 12 kuukauden ikäisille on annettava 2 Varilrix-annosta vähintään 6 viikon välein. Ensimmäisen ja toisen annoksen välinen aika ei saa olla alle 4 viikkoa.
Varilrix-rokotteen ensimmäinen annos voidaan antaa joissain erityistapauksissa 9-11 kuukauden ikäisille imeväisille. Tällöin tarvitaan yhteensä 2 annosta, jotka annetaan vähintään 3 kuukauden välein.
Henkilöt, joilla on riski saada vaikea vesirokko esimerkiksi syöpähoidon takia, voivat saada ylimääräisiä annoksia. Rokotteiden annosväli ei saa missään tapauksessa olla lyhyempi kuin neljä viikkoa.
Annosten antoajan ja lukumäärän päättää lääkäri asianmukaisten virallisten suositusten perusteella.
Yliannostus on hyvin epätodennäköinen, sillä rokote toimitetaan kerta-annosinjektiopullossa ja sen antaa lääkäri tai hoitaja. Muutamia annosteluvahinkoja on raportoitu; vain osaan niistä liittyi poikkeavaa uneliaisuutta ja kouristuskohtauksia.
Ota yhteyttä lääkäriin. Hän päättää, tarvitaanko uusi annos ja milloin se annetaan.
Kuten kaikki lääkkeet, tämäkin lääke voi aiheuttaa haittavaikutuksia. Kaikki eivät kuitenkaan niitä saa. Tämän rokotteen yhteydessä voi esiintyä seuraavia haittavaikutuksia:
Hyvin yleiset (voi esiintyä yli 1 henkilöllä 10:stä):
pistoskohdan kipu ja punoitus.
Yleiset (voi esiintyä enintään 1 käyttäjällä 10:stä):
ihottuma (näppylät ja/tai rakkulat)
pistoskohdan turvotus*
≥ 38 °C kuume (mitattuna peräaukosta)*.
Melko harvinaiset (voi esiintyä enintään 1 käyttäjällä 100:sta):
ylähengitystieinfektio
kurkkukipu ja nielemiskipu (faryngiitti)
imusolmukkeiden suureneminen
ärtyneisyys
päänsärky
uneliaisuus
yskä
nenän kutina, nuha tai nenän tukkoisuus, aivastelu (riniitti)
pahoinvointi
oksentelu
vesirokkomainen ihottuma
kutina
nivelkipu
lihaskipu
> 39,5 °C kuume (mitattuna peräaukosta)
energian puute (väsymys)
yleinen huonovointisuus.
Harvinaiset (enintään 1 käyttäjällä 1 000:sta):
silmän sidekalvotulehdus
vatsakipu
ripuli
kutiseva, paukamainen ihottuma (nokkosihottuma).
Pistoskohdan turvotusta ja kuumetta voi esiintyä hyvin yleisesti nuorilla ja aikuisilla. Turvotusta voi myös esiintyä hyvin yleisesti toisen annoksen jälkeen alle 13-vuotiailla lapsilla.
Varilrixin tavanomaisen käytön yhteydessä on muutamissa tapauksissa raportoitu seuraavia haittavaikutuksia:
vyöruusu (herpes zoster).
vähäinen, pistemäinen verenvuoto tai tavallista herkemmin esiintyvä mustelmanmuodostus, joka johtuu verihiutalemäärän vähenemisestä.
allergiset reaktiot. Ihottuma, joka voi olla kutiseva tai rakkulainen, silmien ja kasvojen turvotus, hengitys- tai nielemisvaikeudet, äkillinen verenpaineen lasku ja tajunnan menetys. Tällaisia reaktioita voi esiintyä jo lääkärin vastaanotolla. Jos sinulla tai lapsellasi esiintyy jokin näistä oireista, ota välittömästi yhteyttä lääkäriin.
aivojen, selkäytimen ja ääreishermoston infektio tai tulehdus, joka aiheuttaa tilapäistä kävelemisvaikeutta (tasapainohäiriö) ja/tai tilapäistä raajojen hallinnan puutetta tai aivohalvauksen (aivojen verenkiertohäiriöstä johtuva aivovaurio).
kouristuskohtaukset.
verisuonien tulehdus, kaventuma tai tukos. Näihin voi liittyä poikkeava verenvuoto tai ihonalainen mustelmanmuodostus (Henoch–Schönleinin purppura) tai kuume, joka kestää yli 5 päivää ja johon liittyy ihottumaa vartalolla ja joskus ihon kuoriutumista käsissä ja sormissa sekä silmien, huulten, kurkun ja kielen punoitusta (Kawasakin tauti).
erythema multiforme (oireena ovat punoittavat, tuhkarokkoa muistuttavat läiskät, jotka usein ovat kutisevia. Läiskät ilmaantuvat ensin raajoihin ja joskus kasvoihin ja koko kehoon).
Jos havaitset itselläsi tai lapsellasi haittavaikutuksia, kerro niistä lääkärille, apteekkihenkilökunnalle tai sairaanhoitajalle. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Voit ilmoittaa haittavaikutuksista myös suoraan (ks. yhteystiedot alla).
Ilmoittamalla haittavaikutuksista voit auttaa saamaan enemmän tietoa tämän lääkevalmisteen turvallisuudesta.
www-sivusto: www.fimea.fi
Lääkealan turvallisuus- ja kehittämiskeskus Fimea Lääkkeiden haittavaikutusrekisteri
PL 55
00034 FIMEA
Ei lasten ulottuville eikä näkyville.
Älä käytä tätä rokotetta kotelossa mainitun viimeisen käyttöpäivämäärän jälkeen. Viimeinen käyttöpäivämäärä tarkoittaa kuukauden viimeistä päivää.
Säilytä ja kuljeta kylmässä (2 C ̶ 8 C). Säilytä alkuperäispakkauksessa. Herkkä valolle.
Käyttökuntoon saattamisen jälkeen rokote tulee injisoida viipymättä.
Jos tämä ei ole mahdollista, käyttökuntoon saatettua rokotetta voidaan kuitenkin säilyttää korkeintaan 90 minuuttia huoneenlämmössä (25 ºC) ja korkeintaan 8 tuntia jääkaapissa (2 ºC – 8 ºC). Rokote on hävitettävä, jos näitä säilytysolosuhteita ei ole noudatettu.
Lääkkeitä ei tule heittää viemäriin, eikä hävittää talousjätteiden mukana. Kysy käyttämättömien lääkkeiden hävittämisestä apteekista. Näin menetellen suojelet luontoa.
Vaikuttava aine: kylmäkuivattuja, heikennettyjä, eläviä varicella-zosterviruksia (Oka-kanta, tuotettu MRC-5 ihmisen diploidisoluviljelmissä). Yksi 0,5 ml annos käyttökuntoon saatettua rokotetta sisältää
> 103,3 PFU:ta (plaque forming units) varicella vesirokkovirusta.
Apuaineet:
Kuiva-aine: aminohappoja (sisältää fenyylialaniinia), vedetön laktoosi, sorbitoli (E420), mannitoli (E421)
Liuotin: injektionesteisiin käytettävä vesi
Injektiokuiva-aine ja liuotin, liuosta varten (injektiokuiva-aine (1 annos) injektiopullossa ja liuotin esitäytetyssä ruiskussa (0,5 ml)) erillisillä neuloilla tai ilman seuraavissa pakkauskoissa:
1 x 1 annos ja 10 x 1 annosta (yksi erillinen neula).
2 erillistä neulaa: 1 x 1 annos ja 10 x 1 annosta.
Ilman neuloja: 1 x 1 annos ja 10 x 1 annosta.
Injektiokuiva-aine on hieman kellertävä, kermanvärinen tai vaaleanpunainen jauhe. Liuotin on kirkas, neste (injektionesteisiin käytettävä vesi) rokotteen käyttökuntoon saattamiseksi.
Kaikkia pakkauskokoja ei välttämättä ole myynnissä.
GlaxoSmithKline Biologicals s.a.,
Rue de l’Institut 89 B-1330 Rixensart Belgia
Lisätietoja tästä lääkevalmisteesta antaa myyntiluvan haltijan paikallinen edustaja. GlaxoSmithKline Oy
Piispansilta 9 A
02230 Espoo
Puh. +358 (0)10 30 30 30
Lisätietoja tästä rokotteesta on saatavilla Lääkealan turvallisuus- ja kehittämiskeskuksen kotisivuilta https://www.fimea.fi.
<------------------------------------------------------------------------------------------------------------------------>
Kuten kaikkia injisoitavia rokotteita annettaessa, saatavilla on aina oltava asianmukainen hoito- ja seurantavalmius siltä varalta, että rokotteen annon jälkeen kehittyy harvinainen anafylaktinen reaktio.
Alkoholin ja muiden desinfektioaineiden on annettava haihtua iholta ennen rokoteinjektion antamista, sillä ne voivat inaktivoida rokotteen sisältämät heikennetyt virukset.
Varilrixia ei saa antaa laskimoon eikä ihon sisään.
Yhteensopivuustutkimusten puuttuessa tätä lääkevalmistetta ei tule sekoittaa muiden lääkevalmisteiden kanssa.
Liuotin ja käyttökuntoon saatettu rokote on tarkastettava silmämääräisesti ennen käyttökuntoon saattamista ja antamista mahdollisten vierasainehiukkasten ja/tai fysikaalisten ominaisuuksien muutosten havaitsemiseksi. Mikäli tällaisia muutoksia havaitaan, liuotinta tai käyttökuntoon saatettua rokotetta ei saa käyttää.
Varilrix -rokote saatetaan käyttökuntoon lisäämällä liuotinta sisältävän esitäytetyn ruiskun koko sisältö injektiokuiva-ainetta sisältävään injektiopulloon.
Lue huolellisesti ohjeet sekä kuvat 1 ja 2 neulan kiinnittämisestä ruiskuun. Varilrix-pakkauksessa oleva ruisku voi hieman poiketa (ilman kierreosaa) kuvassa olevasta ruiskusta. Tällöin neula on kiinnitettävä ilman kiertoliikettä.

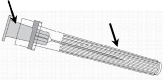
neulan kanta
neulan suoja
Luer Lock -adapteri
Ruiskun mäntä
Ruiskun sylinteri
Ruiskun korkki
Pidä aina ruiskun sylinteristä kiinni, älä pidä kiinni ruiskun männästä tai Luer Lock -adapterista (LLA). Pidä neula samassa linjassa ruiskun kanssa (kuten kuvassa 2). Jos tätä ei tehdä, LLA saattaa vääntyä ja vuotaa.
Jos LLA irtoaa ruiskun kokoamisen aikana, tulee käyttää uutta rokotetta (uusi ruisku ja injektiopullo).
Poista ruiskun korkki kiertämällä sitä vastapäivään (kuten kuvassa 1). Seuraa seuraavia ohjeita riippumatta siitä pyöriikö LLA vai ei:
Kiinnitä neula ruiskuun yhdistämällä kevyesti neulan kanta LLA:iin ja käännä neljäsosakierros myötäpäivään kunnes neula tuntuu lukkiutuvan (kuten kuvassa 2).
Poista neulan suoja, joka voi tuntua jäykältä.
Lisää liuotin injektiokuiva-aineeseen. Seosta on ravistettava hyvin, kunnes injektiokuiva-aine on täysin liuennut liuottimeen.
Vähäisten pH-muutosten vuoksi käyttökuntoon saatetun rokotteen väri voi vaihdella kirkkaan persikanvärisestä vaaleanpunaiseen. Tämä on normaalia, eikä heikennä rokotteen toimintaa. Mikäli muita muutoksia havaitaan, rokotetta ei tule antaa.
Koko injektiopullon sisältö vedetään ruiskuun.
Käytä uutta neulaa rokotteen antamiseen. Poista neula ruiskusta ja kiinnitä injektointiin käytettävä neula toistamalla yllä oleva kohta 2.
Käyttökuntoon saattamisen jälkeen rokote tulee injisoida mahdollisimman pian.
On kuitenkin osoitettu, että käyttökuntoon saatettua rokotetta voidaan säilyttää korkeintaan 90 minuuttia huoneenlämmössä (25 ºC) ja korkeintaan 8 tuntia jääkaapissa (2 ºC – 8 ºC). Rokote on hävitettävä, jos näitä säilytysolosuhteita ei ole noudatettu.
Käyttämätön lääkevalmiste tai jäte on hävitettävä paikallisten vaatimusten mukaisesti.